慢性髓细胞白血病 治疗
慢性髓细胞白血病治疗方法_如何治疗慢性髓细胞白血病
(一)治疗
CML的疗效判断包括血液学缓解、细胞遗传学缓解(即Ph 细胞消失率)和分子生物学缓解(即BCR-ABL融合基因转阴率),由于此三种不同的缓解程度与CML患者的生存期显著相关,因此现代CML治疗的主要目的是如何提高后两者的缓解率,争取患者获得长期无病生存。
1.常规治疗 CML就诊或复发时常有高尿酸症,因此,治疗前应予别 嘌醇300mg/d,口服,并充分补液以维持尿量;如果患者有大量细胞溶解的危险因素,则别 嘌醇给药量及给药次数均应增加,并应维持尿量在150ml/h。由于别 嘌醇可出现过敏性皮炎,因此在白细胞数下降至正常、脾大明显缩小、无明显高尿酸血症后应停用。
2.单药化疗
(1)白消安(马利兰):是第一个广泛应用于CML治疗的化疗药物。其疗效于1968年经随机比较得以肯定。常用剂量为4~6mg/d,口服。由于该药有明显的后效应,因此当白细胞计数下降至30×109/L左右应减量或停药。大部分患者需维持治疗,维持剂量可降至2mg,口服,2次/周,约95%的慢性期患者有效,白细胞计数下降、脾缩小、血细胞比容升高、一般状况恢复正常。
白消安(马利兰)治疗常不能使Ph染色体消失,白消安(马利兰)治疗的目的是控制慢性期,减少死亡率。
该药的主要副作用有严重骨髓抑制、皮肤色素沉着、乏力、发热和腹泻为特征的类似于肾上腺皮质功能不全的综合征和肺纤维化。
(2)羟基脲:1993年通过随机对照系列比较证实羟基脲(HU)优于白消安(马利兰)。其中位生存期删组明显好于BUS组(分别为58个月和45个月),5年生存率分别为44%和32%。由于该药毒性小,可延长CML慢性期和有利于患者进行造血干细胞移植等优点,现已成为CML的首选化学治疗药物。依白细胞计数,起始剂量为1~4g/d,口服;当白细胞下降至20×109/L时改为l~2g/d,维持量为0.5~2.0g/d;当白细胞计数下降至5×109/L时应暂停。HU的副作用轻,可有皮肤丘疹、骨髓细胞巨幼变、大红细胞增多、月经量增多、秃发等,但骨髓抑制少,没有发生肺纤维化者。部分患者可有Ph染色体阳性率减低。最近有研究发现羟基脲(HU)可延缓CML患者骨髓纤维化的发生,对早期轻度纤维化患者有逆转作用。
(3)靛玉红及其衍生物甲异靛:靛玉红和甲异靛是中国医学科学院血液学研究所经过20多年研究首创用于治疗CNL的新药。单用靛玉红100~300mg/d,分3~4次口服,总有效率为95.8%。单用甲异靛75~150mg/d,分3次口服,总缓解率为80.6%。与BUS和HU相比,其缩脾效果明显好于前者。最近,研究证实甲异靛长期疗效与HU相似,甲异靛联合羟基脲(HU)可明显延长患者慢性期,降低患者5年急变率。部分患者可有Ph染色体阳性率减低。主要副作用有不同程度的骨关节疼痛、恶心、纳差、腹痛、腹泻等消化道反应,极少在治疗期间出现骨髓抑制。
(4)其他:国内外有单用环磷酰胺、巯嘌呤(6-巯基嘌呤)、氧芬胂(马法兰)、苯丁酸氮芥(瘤可宁)、二溴甘露醇、乌拉非汀(合520)、秋水仙胺、二溴卫矛醇、卡波醌、三尖杉碱等治疗CML慢性期患者,这些药物虽均对CML有效,但没有一种药物的疗效比BUS或HU好。最近有长疗程高三杉尖酯碱2.5mg/(m2·d),静滴,第1~14天,使6% CML患者获得完全细胞遗传学缓解的报道。
3.干扰素治疗 1983年Talpaz等报道单用天然干扰素(IFN)治疗CML CP患者51例,其中71%(36例)获血液学缓解,且7例(14%)Ph染色体消失。此后关于天然和重组干扰素治疗CML的疗效观察表明血液学缓解率为61%~80%(中位64%),29%~65%的患者有不同程度的细胞遗传学缓解,现已成为CML的首选治疗药物。
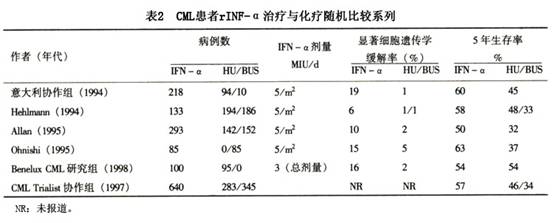
尽管迄今关于干扰素(IFN)治疗CML取得了一些共识:①天然干扰素与重组人干扰素治疗CML疗效相似;②持续用药比间歇用药好,大剂量比小剂量疗效好,初治病例的血液学完全缓解明显比复治者高,加速期的疗效比慢性期差;③肌内注射或皮下注射比静脉注射好。但仍存在诸多问题尚待解决:A. 干扰素(IFN)是否可以延长CML患者生存期:最近发表的干扰素(IFN)治疗CML的大系列随机对照研究结果不一致,意大利协作组和英国MCR的结果显示干扰素(IFN)治疗组较羟基脲(HU)(或白消安(BUS))治疗组生存期明显延长,二者有显著性差异,而德国CML研究组的结果则发现二者生存期并无区别(表2);B. 干扰素(IFN)的最适剂量和用药时间:至今尚无一致意见,但一般为干扰素(IFN)的起始剂量应为5MU/(m2·d),2~3周后剂量增至9~12MU/d,或达到获显著血液学疗效[即WBC计数(2~4)×109/L,血小板计数接近50×109/L]的最大耐受量及患者出现毒性症状需要减少剂量。可望获细胞遗传学缓解的最短时间为6 个月,一般用至病情进展或出现不可耐受的药物毒性;C. 干扰素(IFN)种类与疗效的关系:现一般认为各种不同种类的干扰素a临床疗效无差别,干扰素γ疗效不清,干扰素α联合干扰素γ不能提高疗效;D. 干扰素(IFN)联合其他化疗药物如羟基脲、小剂量阿糖胞苷20mg/(m2·d)×10天已有Ⅱ期临床观察,表明疗效优于单用IFN。
干扰素(IFN)治疗CML的早期常见副反应有发热、畏寒、流感样症状、头痛等,持续约几天至2个月;晚期可有持续乏力、食欲下降、体重下降,少数病例可有贫血、血小板减少、肝肾功能损害、秃发,有时有骨骼、肌肉疼痛及甲状腺功能低下、忧郁等,严重者可有心绞痛、注意力不集中、记忆力减退及昏睡等神经系统毒性表现。剂量减少时以上症状可减轻或消失,给予小剂量解热镇痛药如对乙酰氨基酚(扑热息痛)等可解除上述副作用。
4. 伊马替尼(ST1571、格列卫) 1998年6月伊马替尼(STl57l)(亦称CGP57148或Gleevec)开始Ⅰ期临床试验,共83例干扰素治疗失败的慢性期CML患者,按25~1000mg/d共分14个剂量组接受了治疗,结果证实获最大临床疗效的最低剂量为300mg/d,54例接受300mg/d或以上剂量的患者中53例(98%)获完全血液学缓解,31%的患者获显著细胞遗传学缓解。受此结果鼓舞,58例慢粒急变或Ph 急性白血病患者接受了治疗,剂量为300~1000mg/d,55%(21/38例)的CML急粒变和70%(14/20例)的Ph ALL患者获血液学疗效。其后454例CP CML、181例AP CML和229例CML急粒变患者进入了Ⅱ期临床试验,完全血液学缓解率分别为91%、69%和29%,显著细胞遗传学缓解率分别为55%、24%和16%。2001年5月10日该药获美国FDA批准上市,现正在全球范围进行Ⅲ期临床试验。
伊马替尼(ST1571)的作用机制是抑制BCR-ABL融合基因的酪氨酸激酶活性。迄今,伊马替尼(STl571)的最适临床使用剂量尚不十分明确,CP CML的推荐起始剂量为400mg/d,加速期(急变期)推荐起始剂量为600mg/d,无效患者可增量至800mg/d。由于伊马替尼(STl571)的半衰期为14~16 h,因此1次/d给药即可。主要副作用有骨髓抑制、恶心、肌肉痉挛、骨骼疼痛、关节痛、皮疹、腹泻、水肿、体液潴留和肝功能受损等。
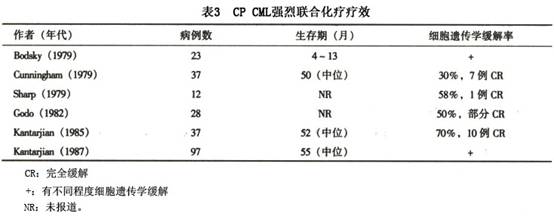
5.联合化疗 采用阿糖胞苷、蒽环类药物、硫鸟嘌呤(6-TG)、环磷酰胺、门冬酰胺酶、巯嘌呤(6-MP)、依托泊苷(VP-16)和白消安(马利兰)等药物组成不同的联合强烈化疗方案治疗CML,Ph染色体减少率高于常规单药治疗。但绝大部分研究表明并不能明显延长生存期(表3)。最近人们又采用联合化疗加 干扰素a疗法试图提高生存率和细胞遗传学缓解率,但迄今结果并不理想。
6.造血干细胞移植(SCT)
(1)自体干细胞移植(ASCT):CP CML患者采用ASCT的结果表明,CP期进行净化干细胞的ASCT能明显延长CML的生存期。
近年来,人们采用联合化疗动员Ph-外周血干细胞,干扰素α单独或联合羟基脲治疗CML等“体内净化”和长期骨髓细胞培养、4-HC和ASTA-Z等药物、干扰素、反义寡核苷酸等“体外净化”方法来筛选Ph-外周血干细胞,尽管使ASCT后Ph转阴率有所提高,但净化干细胞移植患者的生存率并无明显提高。最近,McGlare等总结分析欧美8个BMT中心报告的ASCT治疗CML的效果,200例患者中,CP142例,AP30例,BP或第二次慢性期((CP2)28例,中位年龄42岁,诊断至移植的中位时间为15个月,123例干细胞来源于骨髓,73例来源于外周血,有21例骨髓经体外10天培养净化,23例骨髓经干扰素γ净化,移植后中位随访48个月,CP期移植的患者5年生存率为95%±5%,AP期为27%±10%,而急变后移植的患者全部于移植后2年半内死亡。预后分析表明:年龄>40岁和诊断至移植的时间过长为不利因素,而干细胞来源(骨髓或外周血)及“体外净化”对生存无影响。
(2)异体干细胞移植(Allo-SCT):迄今异体骨髓移植(Allo-BMT)是惟一可以治愈CML的手段。CP移植的存活率比在AP或BP好,且复发率低。CP、AP、BP移植后3年存活率分别为55%~70%、10%~30%、0~20%,复发率分别为20%、50%和75%。BMT前接受过BUS治疗的患者疗效差,且3年无病生存率(DFS)为45%,而接受过HU治疗者则可为61%。IFN-a治疗对BMT治疗疗效无影响。各种预处理方案如Cy+TBI、白消安(BUS)+Cy对疗效无明显影响。Allo-BMT的主要移植相关死亡原因是GVHD。去T细胞Allo-BMT虽然可以降低GVHD发生率,但复发率则明显增高,提示移植物抗白血病(GVL)效应是Allo-BMT治疗CML显示疗效的重要因素。
尽管Allo-BMT治疗CML取得了满意的效果,但仅有20%~25%的患者有HLA匹配的同胞供体。近年来,对无关供体的Allo-BMT治疗CML的研究已取得了可喜的成绩,2年DFS为31%,但其移植失败率高达16%,Ⅲ和Ⅳ级急性GVHD发生率约为54%,严重慢性GVHD亦高达52%。
最近已有研究表明应用异体外周血干细胞移植比Allo-BMT、移植后髓系和免疫重建要快,二者近期疗效相似,远期疗效尚待确定。此外,相关的/无关的脐血移植、非骨髓清除性造血干细胞移植也有初步报道。
为了更好地指导临床选择合适的患者进行异体外周血和骨髓移植,欧洲外周血和骨髓移植组根据3142例患者的资料,提出了预后判定积分系统(表4)。根据该积分系统,积分为0、1、2、3、4、5和6的患者其5年无病生存率分别为72%、70%、62%、48%、40%、18%和22%,移植相关死亡率为20%、23%、31%、46%、51%、71%和73%。
异基因移植后复发患者的治疗包括第2次移植,rIFN-α和供体白细胞输注(donor Leukocyte infusion,DLI可使约75%患者再获CR,血液学复发患者8年存活率可达60%,细胞遗传学复发患者8年存活率约80%,达细胞遗传学和分子生物学疗效的中位时间为4~6个月,那些细胞遗传学/血液学复发者、移植时为第一次慢性期(CPI)、移植后缓解时间1年以上、移植后无慢性GVHD、为嵌合体造血的患者疗效较佳。
7.急变期的治疗 急性髓系细胞变患者可采用原发性AML治疗方案,但CR率<20%,且完全缓解期仅几周或几个月。25%~35%的急变患者为急淋变或双表型白血病变,尽管采用VDLP方案约60%的患者有效,约有1/3患者可返回CP2,但其总生存率亦仅为4~6个月,造血干细胞移植3年DFS可达15%~20%。

8.新的治疗方法
(1)“良性”祖细胞筛选和扩增:已有实验证实在CML患者骨髓CD34 、HLA-DR-组分中可以富集Ph-的造血祖细胞,因此可以据此筛选非白血病性干/祖细胞,通过体外扩增后用于移植。另一种方法是根据“正常”细胞和白血病细胞对细胞因子的不同反应,用干细胞因子缺陷的基质来进行长期培养有利于“良性”细胞增长等特征来进行细胞的功能筛选。可以预测,随着富集和扩增方法的不断改进,富集Ph-细胞进行体外扩增后用于移植是今后CML的治疗方向之一。
(2)反义寡核苷酸:以BCR/ABL为靶标设计的反义寡核苷酸(amtisense oligonucleotide)可以降低BCR/ABL的转录水平和体外培养的CML细胞的增长(可能通过诱导凋亡),现主要用作CML自身干细胞移植的“净化”。已有用BCR/ABL和C-MYB反义寡核苷酸体外净化后骨髓成功植活和获部分细胞遗传学缓解的初步报道。反义寡核苷酸联合化疗药物方案现已在SCID小鼠动物实验证实可显著延缓白血病的发生。
(3)基因治疗:已有用反转录病毒载体构建的BCR/ABL反义基因联合一个甲氨蝶呤(MT)X耐药基因的所谓“双基因治疗策略”的报道,体外实验结果表明该方法可用于CML自身干细胞移植体外净化和移植后化疗,以进一步根除微小残留病。
(4)免疫调节治疗:现已有具有免疫源性的P210 BCR/ABL融合片段和结合主要组织相容性工类抗原等位基因复合物多肽的报道,亦已建立识别BCR/ABL表达细胞的肽特异性CD4 T细胞系,体外实验证实利用肽特异性CD4 T细胞可以使P210 b3a2产物降解。这些结果提示可以用人T细胞介导的肿瘤相关抗原的识别来进行CML的治疗。此外,有治疗潜能的还有白介素-2激活NK细胞和细胞毒T细胞。CML患者自身NK细胞能抑制CML祖细胞生长,因此,可利用自身激活的NK细胞经体外扩增后用于自身干细胞移植净化和CML免疫治疗。最近,又有实验发现CML患者骨髓体外培养获得的树状突细胞能刺激自身细胞,并具有抗增殖作用,而抗正常骨髓活性极低,提示该方法可用于CML的过继免疫治疗。
9.治疗策略的选择 随着CML治疗方法的不断增多,如何根据病人具体情况制订出一个最佳的个体化治疗方案已成为每位血液学工作者面临的一个问题,已提出了几个CML治疗选择模式;最近美国血液学会组织全世界CML专家详尽分析了迄今发表的CML治疗较有价值的文献资料,提出一个CML治疗指南:①首先根据患者年龄、身体状况,是否有相关的或无关的骨髓供体决定是否进行干细胞移植;②如果选择非移植治疗方案则应作出一个详尽的给药方案,如,用rIFN-a,必须对其剂量、疗程是否联用羟基脲或阿糖胞苷作出决定;③应制定一个系统计划来观察细胞遗传学疗效程度和起效时间及分子生物学疗效;④一旦明确了诊断和治疗意见,作出涉及治疗疗效和病人意愿的改动时必须经过审查。
(二)预后
目前尚无可靠的预测方法,但是大量研究证实:年龄、脾脏大小、血小板计数、外周血或骨髓中原始细胞比例、嗜碱性粒细胞比例均为影响预后的因素。1984年Sokal提出一个预测危险比率(risk ratio,RR)的公式,以年龄(年)、脾(肋中线下cm)、血小板数(109/L)及血中原粒细胞数(%)为变量。公式如下:
RR={0.0116(年龄-43.4)+0.0345(脾-7.51)+0.188[(血小板数/700)2-O.563]+0.087(原粒-2.10)}
RR<0.8为低危,RR<0.8~1.2为中危,RR>1.2为高危。有资料表明低危组中位存活期为60个月,中危组为46个月,高危组32个月。但是对于接受IFN治疗的患者,此公式的判断结果不肯定,而对IFN治疗的反应则是影响预后的重要因素。
疾病部位
疾病科室
疾病症状
疾病检查
- 红细胞丙酮酸激酶活性
- 红细胞碱粒凝集试验
- 血清球蛋白(G,GL0)
- 红细胞丙酮酸激酶活性
- 红细胞碱粒凝集试验
- 血清球蛋白(G,GL0)
- 骨髓淋巴细胞系统
- 骨髓红细胞系统
- 骨髓巨核细胞数和分类
- 骨髓有核细胞计数
- 骨髓象分析
- 骨髓细胞增生程度
- 血常规
相关疾病
閺夊繑鐏勯崠璇插悁瀵邦喕淇婇崗顑跨船閸欙拷 xlyd-999


